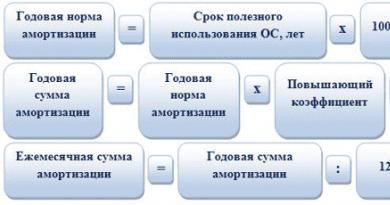
Причины, особенности и методы защиты от электрохимической коррозии. Факторы, влияющие на химическую коррозию
Химическая коррозия - это процесс, состоящий в разрушении металла при взаимодействии с агрессивной внешней средой. Химическая разновидность коррозийных процессов не имеет связи с воздействием электрического тока. При этом виде коррозии происходит окислительная реакция, где разрушаемый материал - одновременно восстановитель элементов среды.

Классификация разновидности агрессивной среды включает два вида разрушения металла:
- химическая коррозия в жидкостях-неэлектролитах;
- химическая газовая коррозия.
Газовая коррозия
Самая частая разновидность химической коррозии - газовая - представляет собой коррозийный процесс, происходящий в газах при повышенных температурах. Указанная проблема характерна для работы многих типов технологического оборудования и деталей (арматуры печей, двигателей, турбин и т.д.). Кроме того, сверхвысокие температуры используются при обработке металлов под высоким давлением (нагревание перед прокаткой, штамповкой, ковкой, термическими процессами и т.д.).
Особенности состояния металлов при повышенных температурах обуславливаются двумя их свойствами - жаропрочностью и жаростойкостью. Жаропрочность - это степень устойчивости механических свойств металла при сверхвысоких температурах. Под устойчивостью механических свойств понимается сохранение прочности в течение продолжительного времени и сопротивляемость ползучести. Жаростойкость - это устойчивость металла к коррозионной активности газов в условиях повышенных температур.

Скорость развития газовой коррозии обуславливается рядом показателей, в числе которых:
- температура атмосферы;
- компоненты, входящие в металл или сплав;
- параметры среды, где находятся газы;
- продолжительность контактирования с газовой средой;
- свойства коррозийных продуктов.
На коррозийный процесс больше влияние оказывают свойства и параметры оксидной пленки, появившейся на металлической поверхности. Образование окисла можно хронологически разделить на два этапа:
- адсорбция кислородных молекул на металлической поверхности, взаимодействующей с атмосферой;
- контактирование металлической поверхности с газом, в результате чего возникает химическое соединение.

Первый этап характеризуется появлением ионной связи, как следствие взаимодействия кислорода и поверхностных атомов, когда кислородный атом отбирает пару электроном у металла. Возникшая связь отличается исключительной силой - она больше, нежели связь кислорода с металлом в окисле.
Объяснение такой связи кроется в действии атомного поля на кислород. Как только поверхность металла наполняется окислителем (а это происходит очень быстро), в условиях низких температур, благодаря силе Ван-дер-Ваальса, начинается адсорбция окислительных молекул. Результат реакции - возникновение тончайшей мономолекулярной пленки, которая с течением времени становится толще, что усложняет доступ кислорода.
На втором этапе происходит химическая реакция, в ходе которой окислительный элемент среды отбирает у металла валентные электроны. Химическая коррозия - конечный результат реакции.
Характеристики оксидной пленки
Классификация оксидных пленок включает их три разновидности:
- тонкие (незаметны без специальных приборов);
- средние (цвета побежалости);
- толстые (видны невооруженным взглядом).
Появившаяся оксидная пленка имеет защитные возможности - она замедляет или даже полностью угнетает развитие химической коррозии. Также наличие оксидной пленки повышает жаростойкость металла.
Однако, действительно эффективная пленка должна отвечать ряду характеристик:
- быть не пористой;
- иметь сплошную структуру;
- обладать хорошими адгезивными свойствами;
- отличаться химической инертностью в отношении с атмосферой;
- быть твердой и устойчивой к износу.
Одно из указанных выше условий - сплошная структура имеет особенно важное значение. Условие сплошности - превышение объема молекул оксидной пленки над объемом атомов металла. Сплошность - это возможность окисла накрыть сплошным слоем всю металлическую поверхность. При несоблюдении этого условия, пленка не может считаться защитной. Однако, из этого правила имеются исключения: для некоторых металлов, например, для магния и элементов щелочно-земельной групп (исключая бериллий), сплошность не относится к критически важным показателям.

Чтобы установить толщину оксидной пленки, используются несколько методик. Защитные качества пленки можно выяснить в момент ее образования. Для этого изучаются скорость окисления металла, и параметры изменения скорости во времени.
Для уже сформированного окисла применяется другой метод, состоящий в исследовании толщины и защитных характеристик пленки. Для этого на поверхность накладывается реагент. Далее специалисты фиксируют время, которое понадобится на проникновение реагента, и на основании полученных данных делают вывод о толщине пленки.
Обратите внимание! Даже окончательно сформировавшаяся оксидная пленка продолжает взаимодействовать с окислительной средой и металлом.
Скорость развития коррозии
Интенсивность, с какой развивается химическая коррозия, зависит от температурного режима. При высокой температуре окислительные процессы развиваются стремительнее. Причем снижение роли термодинамического фактора протекания реакции не влияет на процесс.
Немалое значение имеет охлаждение и переменный нагрев. Из-за термических напряжений в оксидной пленке появляются трещины. Через прорехи окислительный элемент попадает на поверхность. В результате образуется новый слой оксидной пленки, а прежний - отслаивается.

Не последнюю роль играют и компоненты газовой среды. Этот фактор индивидуален для разных видов металлов и согласуется с температурными колебаниями. К примеру, медь быстро поддается коррозии, если она контактирует с кислородом, но отличается устойчивостью к этому процессу в среде оксида серы. Для никеля же напротив, серный оксид губителен, а устойчивость наблюдается в кислороде, диоксиде углерода и водной среде. А вот хром проявляет стойкость ко всем перечисленным средам.
Обратите внимание! Если уровень давления диссоциации окисла превышает давление окисляющего элемента, окислительный процесс останавливается и металл обретает термодинамическую устойчивость.
На скорость окислительной реакции влияют и компоненты сплава. Например, марганец, сера, никель и фосфор никак не способствуют окислению железа. А вот алюминий, кремний и хром делают процесс более медленным. Еще сильнее замедляют окисление железа кобальт, медь, бериллий и титан. Сделать процесс более интенсивным помогут добавки ванадия, вольфрама и молибдена, что объясняется легкоплавкостью и летучестью данных металлов. Наиболее медленно окислительные реакции протекают при аустенитной структуре, поскольку она наиболее приспособлена к высоким температурам.

Еще один фактор, от которого зависит скорость коррозии, - характеристика обработанной поверхности. Гладкая поверхность окисляется медленнее, а неровная - быстрее.
Коррозия в жидкостях-неэлектролитах
К неэлектропроводным жидким средам (т.е. жидкостям-неэлектролитам) относят такие органические вещества, как:
- бензол;
- хлороформ;
- спирты;
- тетрахлорид углерода;
- фенол;
- нефть;
- бензин;
- керосин и т.д.

Кроме того, к жидкостям-неэлектролитам причисляют небольшое количество неорганических жидкостей, таких как жидкий бром и расплавленная сера.
При этом нужно заметить, что органические растворители сами по себе не вступают в реакцию с металлами, однако, при наличии небольшого объема примесей возникает интенсивный процесс взаимодействия.
Увеличивают скорость коррозии находящиеся в нефти серосодержащие элементы. Также, усиливают коррозийные процессы высокие температуры и присутствие в жидкости кислорода. Влага интенсифицирует развитие коррозии в соответствии с электромеханическим принципом.
Еще один фактор быстрого развития коррозии - жидкий бром. При нормальных температурах он особенно разрушительно воздействует на высокоуглеродистые стали, алюминий и титан. Менее существенно влияние брома на железо и никель. Самую большую устойчивость к жидкому брому показывают свинец, серебро, тантал и платина.

Расплавленная сера вступает в агрессивную реакцию почти со всеми металлами, в первую очередь со свинцом, оловом и медью. На углеродистые марки стали и титан сера влияет меньше и почти совсем разрушает алюминий.
Защитные мероприятия для металлоконструкций, находящихся в неэлектропроводных жидких средах, проводят добавлением устойчивым к конкретной среде металлов (например, сталей с высоким содержанием хрома). Также, применяются особые защитные покрытия (например, в среде, где содержится много серы, используют алюминиевые покрытия).
Способы защиты от коррозии
Методы борьбы с коррозией включают:

Выбор конкретного материала зависит от потенциальной эффективности (в том числе технологической и финансовой) его использования.
Современные принципы защиты металла основываются на таких методиках:
- Улучшение химической сопротивляемости материалов. Успешно зарекомендовали себя химически стойкие материалы (высокополимерные пластики, стекло, керамика).
- Изолирование материала от агрессивной среды.
- Уменьшение агрессивности технологической среды. В качестве примеров таких действий можно привести нейтрализацию и удаление кислотности в коррозийных средах, а также использование всевозможных ингибиторов.
- Электрохимическая защита (наложение внешнего тока).
Указанные выше методики подразделяются на две группы:
- Повышение химической сопротивляемости и изолирование применяются до того, как металлоконструкция запускается в эксплуатацию.
- Уменьшение агрессивности среды и электрохимическая защита используются уже в процессе применения изделия из металла. Применение этих двух методик дает возможность внедрять новые способы защиты, в результате которых защита обеспечивается изменением эксплуатационных условий.
Один из самых часто применяемых способов защиты металла - гальваническое антикоррозийное покрытие - экономически нерентабелен при значительных площадях поверхностей. Причина в высоких затратах на подготовительный процесс.

Ведущее место среди способов защиты занимает покрытие металлов лакокрасочными материалами. Популярность такого метода борьбы с коррозией обусловлена совокупностью нескольких факторов:
- высокие защитные свойства (гидрофобность, отталкивание жидкостей, невысокие газопроницаемость и паропроницаемость);
- технологичность;
- широкие возможности для декоративных решений;
- ремонтопригодность;
- экономическая оправданность.
В то же время, использование широкодоступных материалов не лишено недостатков:
- неполное увлажнение металлической поверхности;
- нарушенное сцепление покрытия с основным металлом, что ведет к скапливанию электролита под антикоррозийным покрытием и, таким образом, способствует коррозии;
- пористость, приводящая к повышенной влагопроницаемости.
И все же, окрашенная поверхность защищает металл от коррозийных процессов даже при фрагментарном повреждении пленки, тогда как несовершенные гальванические покрытия способны даже ускорять коррозию.
Органосиликатные покрытия

Химическая коррозия практически не распространяется на органосиликатные материалы. Причины этого кроются в повышенной химической устойчивости таких композиций, их стойкости к свету, гидрофобных качествах и невысоком водопоглощении. Также органосиликаты устойчивы к низким температурам, обладают хорошими адгезивными свойствами и износостойкостью.
Проблемы разрушения металлов из-за воздействия коррозии не исчезают, несмотря на развитие технологий борьбы с ними. Причина в постоянном возрастании объемов производства металлов и все более сложных условий эксплуатации изделий из них. Окончательно решить проблему на данном этапе нельзя, поэтому усилия ученых сосредоточены на поисках возможностей по замедлению коррозионных процессов.
Среди всех существующих видов разрушения металлов наиболее часто встречается электрохимическая коррозия, которая возникает в результате его взаимодействия с электролитически проводящей средой. Основная причина данного явления – это термодинамическая неустойчивость металлов в средах, которые их окружают.

Этому виду коррозии подвержены многие объекты и конструкции:
- газовые и водные трубопроводы;
- элементы транспортных средств;
- другие конструкции, изготовленные из металла.
Коррозийные процессы, то есть, ржавчина, могут возникать в атмосфере, в грунте, и даже в соленой воде. Очистка металлоконструкций от проявлений электрохимической коррозии является сложным и длительным процессом, поэтому проще предотвратить ее возникновение.
Основные разновидности
При коррозии в электролитах происходит преобразование химической энергии в электрическую. В связи с этим ее называют электрохимической. Принято различать следующие виды электрохимической коррозии.
Межкристаллитная
Под межкристаллитной коррозией подразумевается такое опасное явление, при котором происходит разрушение границ зерна никеля, алюминия и других металлов избирательным образом. Как следствие, прочностные и пластичные свойства материала утрачиваются. Главная опасность этой разновидности коррозии в том, что далеко не всегда она заметна визуально.

Питтинговая
Питтинговая электрохимическая коррозия представляет собой точечное поражение отдельных участков поверхности меди и других металлов. В зависимости от характера поражения, различают закрытый, открытый, а также поверхностный питтинг. Размеры пораженных участков могут варьироваться от 0,1 мм до 1,5 мм.

Щелевая
Щелевой электрохимической коррозией принято называть усиленный процесс разрушения металлических конструкций в местах расположения щелей, зазоров и трещин. Протекание щелевой коррозии может происходить в воздушной атмосфере, газовых смесях, а также морской воде. Данный вид разрушения характерен для газопроводов, днищ морских судов и многих других объектов.
Распространено протекание коррозии в условиях небольшого количества окислителя из-за затрудненного подхода к стенкам щели. Это приводит к накоплению коррозийных продуктов внутри зазоров. Электролит, содержащийся во внутреннем пространстве зазора, может изменяться под воздействием гидролиза продуктов коррозии.

С целью защиты металлов от щелевой коррозии принято применять несколько методов:
- уплотнение зазоров и щелей;
- электрохимическая защита;
- процесс ингибирования.
В качестве профилактических методов следует использовать только те материалы, которые в наименьшей степени подвержены возникновению ржавчины, а также изначально грамотно и рационально конструировать газопроводы и другие важные объекты.
Грамотная профилактика во многих случаях представляет собой более простой процесс, чем последующая очистка металлоконструкций от въевшейся ржавчины.
Как проявляется коррозия разных видов
В качестве примера протекания коррозийного процесса можно привести разрушение различных приборов, компонентов автомобилей, а также любых конструкций, произведенных из металла и расположенных:
- в атмосферном воздухе;
- в водах – моря, реки, содержащиеся в почве и под слоями грунта;
- в технических средах и т.д.

В процессе ржавления металл становится многоэлектронным гальваническим элементом. Так, например, если в электролитической среде происходит контакт меди и железа, медь является катодом, а железо – анодом. Отдавая электроны меди, железо в виде ионов попадает в раствор. Ионы водорода начинают двигаться по направлению к меди и там разряжаются. Становясь все более и более отрицательным, катод вскоре приравнивается к потенциалу анода, в результате чего коррозийный процесс начинает замедляться.
Разные виды коррозии проявляются по-разному. Более интенсивно электрохимическая коррозия проявляется в тех случаях, когда в катоде присутствуют вкрапления металла с меньшей активностью по сравнению с корродирующим – на них ржавчина появляется быстрее и является довольно выразительной.
Протекание атмосферной коррозии происходит в условиях влажного воздуха и обычной температуры. В данном случае на поверхности металла образуется пленочка из влаги с растворенным кислородом. Процесс разрушения металла становится интенсивнее по мере увеличения влажности воздуха и содержания газообразных оксидов углерода и серы при условии наличия:
- трещин;
- шероховатостей;
- других факторов, провоцирующих облегчения процесса конденсации.

Почвенная коррозия в наибольшей степени поражает разнообразные подземные сооружения, газопроводы, кабели и другие конструкции. Разрушение меди и других металлов происходит по причине их тесного соприкосновения с почвенной влагой, в составе которой также присутствует растворенный кислород. Разрушение трубопроводов может произойти уже спустя полгода с момента их строительства в том случае, если для почвы, в которой они установлены, характерна повышенная кислотность.
Под воздействием блуждающих токов, исходящих от посторонних объектов, возникает электрическая коррозия. Ее главными источниками являются электрические железные дороги, линии электропередач, а также специальные установки, функционирующие на постоянном электротоке. В большей степени данный вид коррозии провоцирует разрушение:
- газопроводов;
- всевозможных сооружений (мосты, ангары);
- электрокабелей;
- нефтепроводов.
Действие тока провоцирует возникновение участков входа и выхода электронов – то есть, катодов и анодов. Наиболее интенсивным разрушительный процесс является именно на участках с анодами, поэтому на них ржавчина более заметна.
Коррозия отдельных компонентов газопроводов и водяных трубопроводов может быть вызвана тем, что процесс их инсталляции является смешанным, то есть, происходит с использованием различных материалов. Наиболее частыми примерами является точечная коррозия, возникающая в элементах из меди, а также коррозия биметаллов.
При смешанной установке железных элементов со сплавами меди и цинка, процесс коррозии отличается меньшей степенью критичности, чем при медном литье, то есть со сплавами меди, цинка и олова. Предотвратить коррозию трубопроводов можно, используя специальные методы.

Способы защиты от ржавления
Для борьбы с коварной ржавчиной применяются различные методы. Рассмотрим те из них, который являются наиболее эффективными.
Способ №1
Один из самых популярных методов – это электрохимическая защита чугуна, стали, титана, меди и других металлов. На чем же она основывается?
Электрохимическая обработка металлов представляет собой особый способ, направленный на изменение формы, размеров и шероховатости поверхности путем анодного растворения в электролите под воздействием электротока.
Чтобы обеспечить надежную защиту от ржавчины, необходимо еще перед началом эксплуатации металлических изделий обрабатывать их особым средствами, которые в своем составе содержат различные компоненты органического и неорганического происхождения. Данный метод позволяет предотвратить появление ржавчины на определенное время, однако позже придется обновлять покрытие.

Электрозащита представляет собой процесс, при котором металлическая конструкция подключается к внешнему источнику постоянного электрического тока. В результате этого на ее поверхности формируется поляризация электродов катодного типа, и все анодные области начинают преобразовываться в катодные.
Электрохимическая обработка металлов может происходить с участием анода или катода. В некоторых случаях происходит попеременная обработка металлического изделия обоими электродами.
Катодная защита от коррозии необходима в тех ситуациях, когда у металла, подлежащего защите, не наблюдается предрасположенность к пассивации. К металлическому изделию подключается источник внешнего тока – специальная станция катодной защиты. Данный метод подходит для защиты газопроводов, а также трубопроводов водоснабжения и отопления. Однако есть у этого метода определенные недостатки в виде растрескивания и разрушения защитных покрытий – это происходит в случаях значительного смещения потенциала объекта в отрицательную сторону.
Способ №2
Электроискровая обработка металлов может осуществляться при помощи установок различных типов – бесконтактной, контактной, а также анодно-механической.
Способ №3
Для надежной защиты газопроводов и других трубопроводов от ржавчины часто применяется такой метод, как электродуговое напыление. Преимущества данного способа очевидны:

- значительная толщина защитного слоя;
- высокий уровень производительности и надежности;
- применение относительно недорогого оборудования;
- несложный технологический процесс;
- возможность применения автоматизированных линий;
- невысокие энергетические затраты.
Среди недостатков данного метода – невысокая эффективность при обработке конструкций в коррозийных средах, а также недостаточная прочность сцепления со стальной основой в некоторых случаях. В любых других ситуациях такая электрозащита очень эффективна.
Способ №4
Для защиты разнообразных металлических конструкций – газопроводов, мостовых сооружений, всевозможных трубопроводов – требуется эффективная антикоррозийная обработка.

Данная процедура осуществляется в несколько этапов:
- тщательное удаление жировых отложений и масел с применением эффективных растворителей;
- очистка обрабатываемой поверхности от солей, растворимых в воде, – выполняется при помощи профессиональных аппаратов высокого давления;
- удаление имеющихся конструкционных погрешностей, выравнивание кромок – это необходимо для предотвращения сколов наносимого лакокрасочного покрытия;
- тщательная очистка поверхности при помощи пескоструйного аппарата – это делается не только для удаления ржавчины, но и для придания нужной степени шероховатости;
- нанесение противокоррозийного материала и дополнительного защитного слоя.
Правильная предварительная обработка газопроводов и всевозможных металлоконструкций обеспечит им надежную защиту от электрохимической коррозии в процессе эксплуатации.
Лекция 4.
Электрохимическая коррозия представляет собой самопроизвольное разрушение металлов в результате электрохимического взаимодействия с жидкими электролитами, обладающими электропроводностью. Такими электролитами могут быть вода, водные растворы кислот, щелочей, расплавленные соли. Электрохимическая коррозия широко распространена и имеет много разновидностей. Причина электрохимической коррозии-пониженная термодинамическая устойчивость большинства металлов и их стремление переходить в ионное состояние.
При электрохимической коррозии взаимодействие металла с окружающей средой характеризуется анодным и катодным процессами, протекающими на различных участках поверхности металла. Продукты коррозии образуются только на анодных участках.
Электрохимическая коррозия - результат работы коррозионных гальванических элементов. Она происходит следующим образом: на анодных участках протекает реакция окисления с образованием ионов металла Fe 2+ , а на катодных участках под влиянием кислорода образуется гидроокись (как результат протекания реакции кислородной деполяризации). Ионы Fe 2+ и ОН - направляются друг к другу и образуют нерастворимый осадок Fe(OH)2 , который может разлагаться на окись железа и воду. (Fe(OH) 2 ->Fe 2 О 3 +H 2 О). Высвобождающиеся при реакции окисления электроны от анодного участка по металлу изделия перетекают к катодному участку и участвуют в реакции восстановления.
Модель коррозионного микроэлемента представлена на рисунке 4.
С электрохимическим механизмом протекают следующие виды коррозионных процессов:
Коррозия в электролитах – коррозия металлов в жидких средах, проводящих электрический ток. В зависимости от вида электролита различают коррозию в растворах кислот, щелочей и солей (кислотная, щелочная, солевая), в морской, речной воде.
Состав электролита определяет механизм процесса коррозии, влияет на его кинетику и скорость. Например скорость коррозии уменьшается, если электролит содержит анионы или окислители, в результате взаимодействия с которыми на поверхности металла образуется пленка труднорастворимых солей.
Растворенный в электролите кислород оказывает тормозящее или ускоряющее воздействие на процесс коррозии металлов.
На процесс коррозии влияет и концентрация электролита. Практически во всех природных средах с ростом концентрации солей в электролите скорость коррозии сначала возрастает до некоторого максимума, а затем уменьшается в результате снижения растворимости кислорода и затруднения катодного процесса.
Температура электролита также оказывает влияние на скорость коррозии. Это обусловлено тем, что с повышением температуры возрастает электропроводность электролита. С ростом температуры электролита скорость коррозии иногда может возрасти в десятки и сотни раз.
Почвенная коррозия – коррозия подземных металлических сооружений под воздействием почвенного электролита. На поверхности металлических изделий, находящихся в контакте с почвенным электролитом, вследствие местных неоднородностей металла или электролита возникает большое количество коррозионных элементов, природа которых аналогично природе гальванических элементов.
Почвенная коррозия является наиболее распространенным видом электрохимической коррозии, оказывающей воздействие на подземные металлические сооружения. Почвы и грунты чрезвычайно разнообразны не только в пределах больших регионов, но даже и в пределах одного небольшого участка. Между почвой, самым поверхностным слоем земли, и грунтом четкой границы нет.
Биокоррозия – частный случай почвенной коррозии, протекающая под воздействием микроорганизмов, в результате жизнедеятельности которых образуются вещества, ускоряющие коррозионные процессы. В природе наиболее широко распространены сульфатвосстанавливающие анаэробные бактерии, в результате действия которых образуется сероводород, который, соединяясь с железом, дает сернистое железо. Сульфатвосстанавливающие анаэробные бактерии, обычно обитают в воде, грязи, сточных водах, нефтяных скважинах, донных осадках, почве, цементе. Наиболее благоприятной средой для развития этих бактерий являются почвы с (оптимально 6-7,5) при 25-30 0 С. Жизнедеятельность железных аэробных бактерий сопровождается выделением в качестве продуктов коррозии нерастворимой пленки гидроокиси железа.
Биокоррозия (обрастание подводных сооружений морскими растительными и животными организмами - мшанками, балянусами, диатомеями, кораллами) разрушает защитные покрытия и ускоряет разрушение металлов. Некоторые живые организмы (например, мидии) замедляют коррозионный процесс, так как потребляют много кислорода.
Атмосферная коррозия – коррозия металлов в атмосфере воздуха или в среде любого влажного газа. При отсутствии влаги в воздухе железо корродирует с незначительной скоростью.
Она зависит от степени увлажненности поверхности металлов и по этому признаку подразделяется на три типа:
1) мокрая атмосферная коррозия (при относительной влажности воздуха ~ 100 %) при наличии видимой пленки влаги на поверхности металла;
2) влажная атмосферная коррозия при наличии на поверхности металла невидимой пленки влаги, которая образуется при капиллярной адсорбционной или химической конденсации;
3) сухая атмосферная коррозия при полном отсутствии влаги на поверхности металла.
Атмосферы существенно различаются по влажности, температуре и загрязнению, поэтому скорость атмосферной коррозии в различных районах неодинакова, чем ближе к морскому побережью, тем больше воздух насыщен морской солью, в особенности NaCl. В промышленных областях в воздухе появляются значительные количества SO 2 , который превращается в серную кислоту. При работе двигателей внутреннего сгорания в большом количестве образуется NO, который выделяется в атмосферу. В городах и индустриальных центрах в атмосферу выделяется большое количество H 2 S.
По агрессивности атмосферы можно разделить на следующие основные типы: морскую, промышленную, городскую, сельскую, арктическую.
Специфическими факторами, влияющими, на агрессивность атмосферы являются (кроме газов) пыль и влага.
Пленки ржавчины, образующиеся в атмосферных условиях, могут иметь защитные свойства, поэтому скорость коррозии со временем снижается.
В реальных условиях все эти типы коррозии взаимно переходят друг в друга. Характер изменения скорости атмосферной коррозии в зависимости от толщины пленки влаги показан на рисунке. Эта скорость изменяется от нуля для сухой атмосферной коррозии, достигает максимума для влажной атмосферной коррозии и снижается до некоторого постоянного значения, характеризующего скорость коррозии данного металла в электролите.
На скорость атмосферной коррозии металлов влияет большое число факторов:
1) влажность воздуха (создание электролита);
2) примеси воздуха (газы SO 2 , SO 3 , K 2 S, NH 3 , СЬ- НС1 и др. в контакте с водой действуют как депассиваторы, комплексообразователи или катодные деполяризаторы; твердые частицы увеличивают электропроводность пленки электролита и облегчают адсорбцию газов и влаги из воздуха);
3) характер атмосферы (чистая, грязная, сухая, влажная);
4) географическая зона (тропики, субтропики, средняя полоса, пустым, полюс);
5) состояние поверхности корродирующего материала (наличие продуктов коррозии);
6) наличие инородных включений в металле (одни из них защищают от коррозии - катодные включения, например Си, Pb, Pd, а другие способствуют разрушению металла);
7) температура (с повышением температуры скорость коррозии влажность снижаются).
Методы защиты металлов от атмосферной коррозии сводятся следующему:
а) нанесению защитных покрытий (смазки, лаки, пленки, цинкование, никелирование, хромирование, фосфотирование, окисные пленки); б) воздействию на контролирующие процессы (пассивация анода Сг, Al, Ti, Ni, катодные включения Си, Pd); в) уменьшению слоя электролита на поверхности корродирующего металла (осушка и очистка воздуха); г) применению замедлителей коррозии (NaNО 2 , нитриты, карбонаты, бензоаты дициклогексиламина и моноэтаноламина) в основном при хранении металлов и транспортировании их в контейнерах или упаковке из оберточных материалов.
Электрокоррозия – коррозия подземных металлических сооружений, вызванная проникновением на сооружения токов утечки с рельсов электрифицированного транспорта или других промышленных электроустановок и сооружений (электрифицированные железные дороги, метрополитены, линии передачи постоянного тока, установки катодной защиты подземных металлических сооружений).
Эти токи получили название блуждающих, величина и направление их могут изменяться во времени.
Основной величиной, характеризующей интенсивность процесса электрокоррозии, являются сила тока, стекающего с подземного сооружения в грунт, отнесенная к единице поверхности.
Величина тока утечки с подземного сооружения зависит от многих факторов, в частности:
Удельное сопротивление земли;
Величина блуждающих токов в земле;
Взаимное расположение источников блуждающих токов и подземного сооружения;
Состояние внешнего изолирующего покрытия на подземном сооружении;
Продольное сопротивление подземного сооружения.
Контактная коррозия – коррозия, вызванная электрическим контактом двух металлов имеющих различный электрохимический потенциал.
Коррозия под напряжением возникает при одновременном воздействий коррозионной среды и механических напряжений в металле.
Щелевая коррозия – ускорение коррозионного разрушения металла электролитом в узких зазорах и щелях (в резьбовых и фланцевых соединениях).
Коррозионная эрозия – при одновременном воздействии коррозионной среды и трения.
Коррозионная кавитация возникает при одновременном коррозионным и ударном воздействии окружающей среды (коррозия лопаток рабочих колес центробежных насосов, разрушение лопаток гребных винтов на судах).
Фреттинг – коррозия представляет собой локальное коррозионное разрушение металлов при воздействии агрессивной среды в условиях колебательного перемещения двух трущихся поверхностей относительно друг друга.
Структурная коррозия обусловлена структурной неоднородностью сплава. При этом происходит ускоренный процесс коррозионного разрушения вследствие повышенной активности какого–либо компонента сплава.
Термоконтактная коррозия возникает за счет температурного градиента, обусловленна неравномерным нагреванием поверхности металла.
На скорость химической (газовой) коррозии металлов и сплавов влияют внешние и внутренние факторы.
К внешним факторам относятся состав и давление газовой среды, скорость её движения, температура, режим нагрева.
Состав газовой среды . При высоких температурах металлы взаимодействуют с кислородом, парами воды, оксидом углерода (lV), оксидом серы (lV) по схеме
2М + О 2 = 2МО,
М + СО 2 = МО + СО,
М + Н 2 О = МО + Н 2 ,
3М + SО 2 = 2МО + МS.
Скорости этих химических реакций и защитные свойства образующихся плёнок различны, следовательно, скорости коррозии металлов в указанных средах также различны.
Из экспериментальных данных известно, что при 900 0 С ско-рость окисления Fe, Co, Ni возрастает в ряду
Н 2 О (П) ® СО 2 ® О 2 ® SО 2
В отличие от этих металлов Cu практически не корродирует в атмосфере SO 2 .
В приведенных выше газах скорость газовой коррозии металлов увеличивается в ряду
Cr ® Ni ® Co ® Fe
Вольфрам при 900 0 С наибольшую скорость коррозии имеет в атмосфере О 2 , а наименьшую ─ в СО 2 .
Загрязнение воздуха СО 2 , SО 2 , парами Н 2 О вызывает повышение скорости коррозии малоуглеродистой стали. Это связывают с увеличением несовершенств в оксидной плёнке.
При нагревании стали в атмосфере, содержащей О 2 , СО 2 , Н 2 О, помимо окисления, может происходить обезуглероживание (декарбонизация)
Fe 3 C + 1/2O 2 = 3Fe + CO,
Fe 3 C + CO 2 = 3Fe + 2CO,
Fe 3 C + H 2 O = 3Fe + CO + H 2 .
Наводороживание стали происходит при высоких температурах адсорбированными на её поверхности атомами водорода. При комнатной температуре молекулы Н 2 не диссоциируют, поэтому наводороживания стали не происходит. Наводороживание вызывает резкое уменьшение пластичности, понижает длительную прочность металлов. Склонен к наводороживанию титан.
Температура . Повышение температуры вызывает увеличение константы скорости химической реакции, а также рост скорости диффузии реагентов в плёнке продуктов коррозии. Это приводит к увеличению скорости газовой коррозии металлов и сплавов ─ Fe, Cu, и др.
Температура может оказывать влияние на состав образующихся плёнок и закон их роста (таблица 1).
Большое влияние на скорость окисления оказывает режим нагрева. Колебания температуры при нагреве и особенно попеременный нагрев и охлаждение вызывают разрушение плёнки вследствие возникновения больших внутренних напряжений, в результате чего скорость окисления металлов увеличивается.
Таблица 1 ─ Влияние температуры на состав и закон роста оксид-
ных плёнок
Давление газа . С повышением парциального давления кислорода скорость коррозии металлов возрастает.
Для некоторых металлов и сплавов при постоянной достаточно высокой температуре с увеличением парциального давления кислорода скорость окисления сначала растёт, а затем при достижении некоторого критического значения Ро 2 ─ резко уменьшается (рисунок 7) и в широком диапазоне давлений остаётся достаточно низкой.

Р О 2 КР Р О 2
Рисунок 7 - Влияние парциального давления кислорода на
скорость газовой коррозии
Явление уменьшения скорости газовой коррозии при повышении парциального давления кислорода называют высокотемпературной пассивацией. Пассивное состояние металла связывают с образованием на его поверхности совершенной плёнки.
Высокотемпературную пассивацию имеют хромистые стали, медь, титан, цинк и другие металлы и сплавы.
При значительном увеличении парциального давления кислорода выше критического, у целого ряда нержавеющих сталей, например, 08Х13 (Х13), 30Х13 (Х13), 12Х17 (Х17), 08Х18Н10Т (Х18Н10Т) происходит нарушение пассивного состояния («перепассивация»), что приводит к увеличению скорости окисления.
Увеличение скорости коррозии при высоких температурах может вызвать повышение скорости движения газовой среды.
К внутренним факторам, влияющим на скорость химической коррозии металлов относятся: природа, химический и фазовый состав сплава, механические напряжения и деформация, характер обработки поверхности.
Состав и структура сплава . Скорость окисления сталей при высоких температурах с повышением содержания углерода понижается. Уменьшается обезуглероживание сталей. Это связано с интенсификацией процесса образования оксида углерода (II). Сера и фосфор практически не влияют на скорость окисления стали.
На скорость коррозии стали, в кислородсодержащей среде влияют легирующие элементы. Хром (Cr), алюминий (Al) и кремний (Si) сильно замедляют процесс окисления стали. Это связано с обра-зованием плёнок с высокими защитными свойствами. При содержании приблизительно 30 % Cr, до 10 % Al, до 5 % Si, стали имеют высокую жаростойкость. Меньшее повышение жаростойкости дает легирование стали титаном (Ti), медью (Cu), кобальтом (Со) и бериллием (Be).
Элементы, образующие легкоплавкие или летучие оксиды, например, ванадий (V), молибден (Мо), вольфрам (W) ускоряют оки-сление стали.
Высокой жаростойкостью обладают сплавы никеля (Ni) c хромом (Сr) - нихромы. Типичные нихромы содержат 80 % Ni и 20 % Cr или 65 % Ni, 20 % Cr и 15 % Fe.
Скорость окисления меди (Cu) понижается при её легировании Al, Be, оловом (Sn) и цинком (Zn).
На скорость коррозии влияет также структура сплава . Установлено, что наиболее жаростойкой является сталь с аустенитной (однофазной) структурой. Хромоникелевые стали с двухфазной аустенитно-ферритной структурой менее устойчивы к окислению. С увеличением содержания ферритной составляющей скорость окисления стали повышается. Например, хромоникелевая аустенитная сталь 12Х18Н9Т (Х18Н9Т) имеет более высокую жаростойкость, чем двухфазная сталь Х12Н5Т с более высоким содержанием хрома. Это связывают с тем, что на двухфазных сталях образуются менее совершенные плёнки, чем на однофазных.
Жаростойкость чугуна зависит от формы графитовых выделений. При шаровидной форме графита жаростойкость чугуна выше.
Деформация металлов в процессе нагрева может вызвать нарушение сплошности плёнок и связанное с этим увеличение скорости окисления. Повышенная шероховатость поверхности металла способствует образованию защитных плёнок с дефектами, что ведет к увеличению скорости коррозии.
Электрохимическая коррозия представляет собой процесс разрушения металла в результате воздействия на него гальванических элементов, образование которых становится возможным в коррозионной среде.
1
Обычно под коррозией металла понимают его окисление под влиянием кислот, которые присутствуют в растворах, контактирующих с металлическим изделием, либо кислорода воздуха. Коррозия наиболее часто поражает металлы, находящиеся левее водорода в так называемом ряду напряжений. Впрочем, коррозионному разрушению подвержены и многие другие материалы (неметаллические), например строительный бетон.
Коррозия возникает в результате какого-либо электрохимического или химического процесса. По этой причине ее принято подразделять на электрохимическую и химическую.
Коррозия приводит к различным разрушениям материала, которые могут быть:
- неравномерными и равномерными;
- местными и сплошными.
Если металл испытывает механические напряжения в дополнение к негативному влиянию внешней среды, наблюдается активизация (и существенная) всех коррозионных проявлений, что вызвано разрушением на поверхности изделий оксидных пленок и уменьшением показателя термоустойчивости материала.

Стоит сказать, что в некоторых случаях коррозионные процессы вызывают восстановление, а не окисление компонентов, входящих в различные металлические сплавы. Ярким примером этого является восстановление водородом содержащихся во многих сталях карбидов (такой нестандартный процесс происходит при высоких температурах и давлениях).
2
Такая коррозия признается наиболее распространенной. Появляется она в том случае, когда среда, характеризуемая электролитической проводимостью, взаимодействует с металлом. Другими словами, ее первопричиной можно смело называть неустойчивость (термодинамическую) металлов в средах, где они находятся. Известные любому человеку примеры такой коррозии – ржавление на открытом воздухе конструкций и изделий из чугуна и разных марок стали ( , и так далее), днищ судов в морской воде, инженерных коммуникаций и трубопроводов, по которым транспортируются разнообразные жидкости и агрессивные составы.

Коррозионный элемент (его обычно называют гальваническим) образуется тогда, когда два металла, имеющие разные потенциалы (окислительно-восстановительные), соприкасаются. Такой элемент – это обычная гальваническая ячейка замкнутого типа. В указанной ячейке металл с меньшим потенциалом медленно растворяется, а второй компонент (с большим потенциалом) обычно не изменяет своего состояния.

Подобным изменениям чаще всего подвергаются металлы, у которых величина отрицательного потенциала высока. В них процесс ржавления (формирования коррозионного компонента) начинается уже тогда, когда на поверхность попадает малый объем постороннего включения.
3
Описанные гальванические элементы образуются по разным причинам. Прежде всего, они могут формироваться из-за неоднородности сплава, что приводит к:
- неравномерности распределения пленок оксидов на поверхности материала;
- неоднородности металлической фазы;
- присутствию кристаллов на границах зерен;
- различиям в процессе формирования вторичных продуктов ржавления;
- анизотропности кристаллов.

Также гальванические ячейки возникают в силу следующих причин:
- неоднородности температуры, влияний внешних токов и облучения;
- наличия зон, в которые окислитель поступает ограниченно.
Всегда нужно помнить о том, что электрохимическое ржавление подразумевает протекание в один и тот же момент времени двух процессов – анодного и катодного. С точки зрения кинетики они напрямую связаны между собой. Основной металл всегда растворяется на аноде (окислительная реакция).

Под катодным процессом понимают ситуацию, когда "лишние" электроны поглощаются атомами либо молекулами электролита. После чего происходит восстановление электронов. Катодный процесс замедляется, если отмечается замедление анодного процесса. Как видим, механизм электрохимической коррозии совсем несложен для понимания. Разобраться с ним может любой человек.
4
Под таким явлением понимают разрушение металла, вызываемое контактом коррозионной среды и материала. Причем при подобном взаимодействии наблюдается сразу два процесса:
- коррозионная среда восстанавливается;
- металл окисляется.
Электрохимическая коррозия металлов отличается от химической тем, что последняя протекает без электротока. А первопричина этих видов коррозии, коей является термодинамическая неустойчивость, остается неизменной. Металлы легко переходят в разные состояния (включая и более устойчивые), причем в этом случае отмечается снижение их термодинамического потенциала.

- в жидких составах, которые не причисляются к электролитами;
- газовая.
К жидкостям-неэлектролитам относят составы неспособные проводить электроток:
- неорганические: сера в расплавленном состоянии, жидкий бром;
- органические: бензин, керосин, хлороформ и иные.
Неэлектролиты в чистом виде с металлами не контактируют. Но при появлении в жидкостях совсем малого числа примесей сразу же "стартует" химическая коррозия металлов (причем весьма бурная). В тех ситуациях, когда реакция проходит еще и при повышенных температурах, ржавление будет происходить намного интенсивнее. А если в неэлектролитические жидкости попадает вода, запускается механизм электрохимической коррозии, описанный нами выше.

Процесс ржавления (химического) чаще всего идет в пять этапов:
- сначала к поверхности металла подходит окислитель;
- на поверхности стартует хемосорбция реагента;
- после этого начинает формироваться оксидная пленка (взаимодействие металла и окислителя);
- отмечается десорбция материала и оксидов;
- фиксируется диффузия в жидкость-неэлектролит оксидов.
Два этапа, указанные последними, отмечаются не каждый раз.
5
Под воздействием газов металлические поверхности могут разрушаться в том случае, когда имеется высокая температура. Данное явление специалисты именуют газовой коррозией, которая признается самым распространенным вариантом химического ржавления. Известная всем вариация подобного процесса – контакт кислорода и металлической поверхности, которая характеризуется двумя показателями:
- давлением при конкретной температуре диссоциации оксидных паров;
- давлением (парциальным) кислорода.

Если давление кислорода меньше давления диссоциации, появляется чистый металл, если больше – образуется окисел. При равных величинах реакция будет полностью равновесной. Учитывая это, можно без труда рассчитать, при каких температурах возникнет опасность коррозии.
Химическая коррозия протекает с разной скоростью. Конкретная величина последней находится в зависимости от далее приведенных факторов:

- свойства продуктов коррозии;
- особенности газовой среды;
- температура;
- время, на протяжении коего отмечается взаимодействие металла со средой;
- виды и состав сплавов либо особенности металла.